盖蒂图片社
2021年6月7日美国食品和药物管理局(FDA)批准Aduhelm (aducanumab的治疗阿尔茨海默氏症这是一种影响620万美国人的衰弱疾病。Aduhelm被批准使用加快审批途径这种药物可以用于治疗严重或危及生命的疾病,比现有的治疗方法具有明显的治疗优势。加速批准可以基于药物对替代终点的影响,合理地预测对患者的临床效益,并要求在批准后进行试验,以验证药物提供预期的临床效益。
“阿尔茨海默氏症是一种毁灭性的疾病,它会对确诊患者及其亲人的生活产生深远影响,”他说帕特里齐亚·卡瓦佐尼,医学博士他是FDA的主任药物评价与研究中心."目前可用的疗法只治疗该疾病的症状;这种治疗方案是针对和影响阿尔茨海默症潜在疾病过程的第一种治疗方法。正如我们从与癌症的斗争中所学到的,加快审批途径可以更快地为患者带来治疗,同时刺激更多的研究和创新。”
阿尔茨海默氏症是一种不可逆转的、进行性的大脑疾病,它会慢慢破坏记忆和思维能力,最终破坏完成简单任务的能力。虽然阿尔茨海默病的具体病因还不完全清楚,但它的特征是大脑发生变化,包括淀粉样斑块和神经纤维(tau)缠结,这导致神经元及其连接的丧失。这些变化会影响一个人的记忆和思考能力。
Aduhelm是首个被批准用于治疗阿尔茨海默症的药物。这是自2003年以来批准的首个针对阿尔茨海默症的新疗法,也是首个针对该疾病基本病理生理学的疗法。
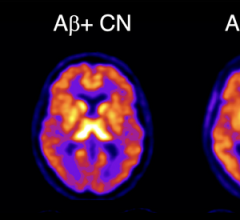
研究人员在三个独立的研究中评估了Aduhelm的疗效,共代表了3482名患者。这些研究包括双盲、随机、安慰剂对照剂量范围的阿尔茨海默病患者研究。接受治疗的患者的β淀粉样蛋白斑块有显著的剂量依赖性和时间依赖性减少,而对照组患者的β淀粉样蛋白斑块没有减少。
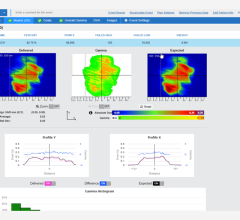
这些结果支持加速批准Aduhelm,这是基于大脑淀粉样β斑块减少的替代终点——阿尔茨海默病的标志。淀粉样斑块定量使用正电子发射断层扫描(PET)成像来估计脑淀粉样蛋白斑块的水平,该斑块在复合脑区中,预计将广泛受阿尔茨海默病病理影响的脑区与预计不会受这种病理影响的脑区进行比较。
Aduhelm的处方信息包括淀粉样相关成像异常(ARIA)的警告,这种异常通常表现为大脑区域的暂时性肿胀,通常随着时间的推移会消失,但不会引起症状,尽管有些人可能会出现头痛、意识模糊、头晕、视力改变或恶心等症状。另一个对Aduhelm的警告是有过敏反应的风险,包括血管性水肿和荨麻疹。Aduhelm最常见的副作用是ARIA、头痛、跌倒、腹泻和精神错乱/谵妄/精神状态改变/方向感障碍。
根据加速批准条款,为患有这种疾病的患者提供更早获得治疗的机会,FDA要求该公司,生原体进行一项新的随机对照临床试验,以验证该药物的临床效益。如果试验未能证实临床疗效,FDA可能启动程序撤回对该药物的批准。
阿杜黑姆得到了许可快速通道该指定旨在加快开发和审查旨在治疗初步证据显示有潜力解决未满足医疗需求的严重疾病的药物。
FDA的裁决是在临床试验有争议的结果之后做出的。在两项III期临床试验中,只有一项试验达到了研究的主要终点:临床衰退的减少。然而,两项研究都显示β -淀粉样蛋白斑块显著减少,这表明未来临床衰退可能会减少。
核医学与分子成像学会(SNMMI)对核医学有机会支持这种新药的精确诊断和治疗效果感到兴奋。“Aduhelm的批准对阿尔茨海默症患者及其家人来说是一个巨大的胜利。在这种情况下,药物的潜在好处肯定大于风险。”SNMMI总统艾伦·帕卡德博士,在一份书面声明中。“我们对此感到自豪核医学可以通过提供明确的诊断和监测治疗的有效性来帮助支持这种药物。”
超过600万美国人患有阿尔茨海默氏症,随着人口老龄化,这个数字预计还会增加。它是美国成年人死亡的第六大原因。
Aduhelm由Biogen和Eisai株式会社生产。两家公司计划在全球销售该药。
欲了解更多信息:www.fda.gov


 2022年10月21日
2022年10月21日



![奥林巴斯宣布全球推出EVIS EUS内镜超声中心EU-ME3。[图片来源:奥林巴斯公司]](http://www.alohadebbie.com/sites/default/files/styles/feed_medium/public/Olympus_0.jpg?itok=0mBwM7Gg)