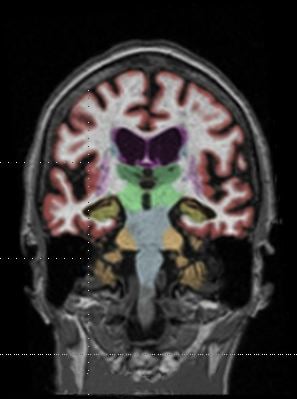
如图所示,钆造影剂(gbca)部分保留在大脑中,引起了安全问题。
近年来放射学中最大的担忧之一是用于放射治疗的钆基造影剂(gbca)的安全性核磁共振成像.几年前,放射科医生和患者开始质疑钆的安全性,当时2014年底的一项研究表明,这种物质会沉积并保留在大脑中再加上一小部分患者声称他们的健康在钆检查后受到了损害,这在放射学中引发了关于这些药物安全性的大争论。
在去年11月举行的2017年北美放射学会(RSNA)会议上,ITN在几次会议上提出了这个问题,并与专家进行了交谈。很明显,在RSNA,许多放射科医生担心钆沉积和钆毒性的可能影响。
他说:“已经有患者报告说,他们认为钆造影剂有副作用,这引起了我们作为放射科医生的注意。马克斯·温特马克,医学博士放射学教授和神经放射学主任,斯坦福医院和诊所.“我每周都会接到很多患者的电话,他们都很担心,所以我们就风险与收益进行了讨论。”
众所周知,肾功能不全的患者无法从体内过滤钆,因此美国食品和药物管理局(FDA)在造影剂包装上标注了警告标签。但是,几乎没有证据表明肾功能正常的患者存在安全问题。方框警告还包括已知的过敏关系,可能发生,特别是在过敏性疾病的患者。
在社交媒体上有许多患者创建的讨论核磁共振成像的小组钆毒性这些问题提高了公众对可能与以前未知的钆副作用有关的话题的认识。对这些患者来说,最大的公关推动因素是2017年11月的动作片演员罗礼士提起了诉讼指控一名造影剂供应商和造影剂分销商毒死他的妻子吉娜。她做了几次核磁共振造影检查,诉讼称这些检查后开始出现许多不良健康影响。诺里斯要求1000万美元的赔偿
诉讼称,她感染了所谓的“钆沉积病”。这是一个经常被那些声称自己在磁共振造影检查中出现慢性健康问题的患者使用的术语。然而,医学界的许多人并不接受这个术语,因为缺乏科学证据表明它与造影剂有直接联系。该诉讼描述了Gena的症状:全身灼痛、剧烈颤抖、麻木、刺痛、虚弱、认知障碍、肾损伤和呼吸困难。这些症状与患者社交媒体群中经常报道的其他症状相似。
“这起诉讼将提高公众的意识,以及由此带来的所有积极和消极后果,”他说Emanuel Kanal,医学博士匹兹堡大学医学中心的核磁共振服务主任和放射学和神经放射学教授,RSNA这一主题的主要发言人之一。“负面结果是,当患者真的非常需要造影剂检查时,他们可能会选择不做造影剂检查,从而导致歇斯底里。患者的潜在好处是巨大的,不做造影剂检查可能真的会对他们造成伤害。”他说,公众意识的积极一面是,它将促使更多的问题通过临床研究得到解答,以确保医学界对这些药物有更好的了解。他说:“当患者询问我们正在使用的药物时,我们需要能够做出回应。”
缺乏证据表明钆的危害
医生们在很大程度上不愿意将钆剂与这些疾病直接联系起来,因为几乎没有临床证据表明两者之间存在直接联系。不同患者报告的症状也有很大差异。温特马克说,在过去的几十年里,钆造影剂已经被用于成千上万的患者,临床证据表明它对大多数患者是安全的。直到过去几年,人们还不知道钆会在组织中积累和保留,尤其是在大脑中。温特马克说,以前人们认为这种毒剂会完全从体内排出。他说,一些大规模的研究正在进行中,但需要时间来收集数据,以确定钆滞留的长期影响。
“我不完全相信钆没有毒性,”Kanal说。“我还不知道该怎么办。问题是缺乏显示毒性的数据,但大量数据显示它是安全的。”
在RSNA会议上,其他发言者也反映了缺乏显示患者伤害的证据。
“我们不知道临床意义是什么,这就是为什么我们继续对此进行临床研究的原因,”拜耳医疗保健美国医疗事务的Sheela Agarwal医学博士在拜耳主办的RSNA午餐会上就钆安全性问题发表了讲话。她说,在过去的几年里,已经有大约50项关于这个主题的研究,但没有一项研究提供了确凿的证据,表明钆潴留会导致慢性疾病。她解释说:“作为临床医生,如果我们不能明确地将因果关系联系起来,就很难将某种疾病称为疾病。”
FDA在钆毒性问题上做了什么?
FDA同意需要进行更多的研究,而且没有足够的证据来对gbca进行监管。2017年9月,FDA医学影像药物咨询委员会(MIDAC)以压倒性多数投票建议在钆造影剂(gbca)上添加新标签,警告钆可能在体内滞留。[3]标签将进一步解释线性gbca比大环药物具有更大的风险,并且对某些患者人群具有更大的风险。2017年12月,FDA在一份药物安全沟通中宣布,要求所有gbca上都包含这些新的警告FDA还呼吁加强对患者的教育,并要求钆造影剂供应商进行额外的动物和临床研究,以评估这些药物的安全性。
FDA表示,目前没有临床证据表明钆滞留与肾功能正常患者的不良健康影响有直接联系,FDA已得出结论,所有已批准的gbca的益处继续超过任何潜在风险。
“对健康的影响,如果有的话,目前还完全未知,到目前为止还没有已知的钆残留的后果,”卡纳尔说。“这并不意味着没有,这只是意味着我们现阶段还不知道有,需要更多的研究。这似乎是FDA和MIDAC委员会到目前为止的结论。”他说,美国放射学会和国际磁共振医学学会也得出了类似的结论。
然而,2017年7月,欧洲药品管理局(EMA)发布了最终意见,建议限制一些线性钆基造影剂(gbca)的使用,并暂停其他产品的销售许可,理由是担心钆沉积。[5]但是,EMA表示支持继续使用大环gbca。EMA表示:“目前没有证据表明大脑中的钆沉积对患者造成了任何伤害。然而,EMA建议限制一些静脉线性药物,以防止任何可能与钆脑沉积相关的风险。”
EMA建议暂停GBCAs Magnevist (gadopentetate dimeglumine)、Omniscan (gadodiamide)和OptiMark (gadoversetamide)的市场许可。该小组指出,收益-风险平衡对某些线性gbca不再有利。但是,EMA认为某些线性gbca仍然需要用于肝脏成像,因此保留了Primovist(美国Eovist, gadoxetate二钠)和MultiHance (gadoxetate diglumine)。
卡纳尔指出,ACR去年秋天发表了一份声明,不同意EMA的建议。卡纳尔解释说:“从固定数量的数据来看,大西洋两岸得出了非常不同的结论。”“多项进一步研究显然是有必要的。”
钆沉积知多少
根据其化学形状,有两类gbca -线性和大环剂。Agarwal说,有四项研究[6,7,8,9]表明线性药物比大环药物在大脑中有更多的保留。然而,最近的研究也表明,包括大环在内的所有药物都会在大脑中留下一定程度的钆。她说,虽然近年来大脑中的沉积一直是人们担忧的主要原因,但在动物实验中,皮肤和骨骼中保留的钆含量是大脑中钆含量的100倍。
卡纳尔说:“几十年来,我们已经知道这些制剂在人体内有残留量,而且水平因制剂而异。”“但是,不管出于什么原因,当神田博士在2013年12月表明大脑部分区域的磁化行为发生了变化时,然后文献继续发现它与钆的存在有关,这引起了大量的反应和担忧。”
Kanal说,为了降低钆的毒性,它与另一种伴侣或配体分子放在一起。他解释说,这种钆分子的螯合极大地提高了安全指数,并允许它用作人体造影剂。然而,卡纳尔说,对于保留在体内的钆,有一种理论认为,只要这种物质保持螯合、囚禁的形式,它就是安全的。
他解释说:“但是,如果钆从配体分子上脱落,就可能导致诸如肾源性全身性纤维化(NSF)等疾病。”“现在有些人想知道同样的事情是否适用于大脑。但是,大脑是不同的,它不能通过纤维化来治愈损伤,大脑是通过胶质细胞增生来治愈的。所以,我们甚至不确定钆以什么形式存在会有危险,如果有危险的话。我们现在还不太清楚。有巨大的压力说,当它分离时,它就会成为一个问题,并导致NSF。”他说,这个事实可能是正确的,但你不能自动地假设,当钆从螯合分子中分离时,它会导致其他问题。
“今天,还有大量的东西我们仍然不知道。但是,仅仅因为我们没有看到任何伤害,并不意味着没有任何伤害,仅仅因为它分离,并不意味着它对那个器官有任何伤害。”他说,当钆分离时,它可能会进入磷酸盐或碳酸盐,磷酸钆可能会沉淀到大脑的基底神经节。“但是,钙,我们所知道的另一种金属,在大脑中析出,这是一个正常的发现,”他说。即使大脑中有某种形式的钆沉淀,问题是它是惰性的还是真的有害。“我们没有办法知道,在这个阶段说还为时过早。但是,令人担忧的是,我们发现,在我看来,这个行业很难将知识与意见和炒作区分开来。”“但是,我认为每个人都会同意,如果我们的体内没有任何残留的钆会更好。”
他说,有一种趋势是将所有大环制剂和线性制剂归为一类,并说这些制剂的作用都是一样的。但是,最近的研究表明,即使在同一类代理中,也不都表现相同,因此不应该将它们归为一类。
放射科医生现在能对钆做些什么
Kanal说,新的公众意识将迫使放射科医生开始在检查前亲自批准所有对比剂剂量,以确保它们是合理的,权衡每个患者的风险收益。他说,放射科医生不应该依赖那些安排检查的医生,这些医生不知道这些药物之间的区别,也真的不了解潜在的安全问题。
“这些是药物制剂,这些是我们的病人,”卡纳尔说。“我们不仅仅是‘医生的医生’,从字面上和法律上讲,这些都是我们的病人,作为一名放射科医生,我将对我对病人所做的每一个决定承担法律责任。我所做的每一个决定,无论是作为还是疏忽,都是我自己的决定。如果我因为转诊医生开的药而允许开某种药,那也是我的法律责任,如果有伤害,那就是责任。”
匹兹堡大学(University of Pittsburgh)有一个流程,在扫描患者之前,放射科医生需要审查所有要求对比检查的订单,以获得最终批准。Kanal是做紧急放射学的,大约五分之一的要求造影剂的订单被取消了,因为不需要造影剂或核磁共振成像。
温特马克说:“(在斯坦福大学)我们检查每一次核磁共振检查,我们检查检查的指征,过去的病史,我们检查以前的成像。”“在那之后,我们会制定每项研究的方案,并试图决定什么对患者是最好的。无论何时我们使用这些造影剂,我们都要确保对患者有明显的好处。就像我们在医学上使用的任何东西一样,它总是有好处的,但也有潜在的风险,作为放射科医生,我们需要与患者一起决定什么对他们来说是最好的。”
需要钆剂量追踪,病人登记
以科学的形式跟踪钆制剂安全性的一种方法是建立患者登记处。患者数据、造影剂剂量、使用的药物类型、MRI系统、使用的方案和患者病史都可以包括在注册数据中,因此当患者说他们正在经历健康问题或潜在的不良反应时,可以在大量人群中进行跟踪,以确定相似性。
许多类型的植入式设备已经做到了这一点,在某些情况下,FDA要求进行上市后监督,医学协会作为第三方托管和管理注册数据收集。
Kanal说:“我认为在不久的将来很可能会建立一个患者登记处。”
然而,放射学面临的一个大问题是,目前大多数部门都没有记录造影剂的剂量,甚至没有记录使用了什么特定的药物。阿加瓦尔说:“很难从EMR中找出有多少次使用了钆造影剂或使用了多少剂量。”
卡纳尔说:“在过去,放射学作为一门专业,在准确记录我们给了多少药,甚至是我们给了什么药方面,一直是一个糟糕的失败。”然而,他预计,由于目前人们对钆的担忧,造影剂的治疗将会迅速而大规模地变得更像处方药。这包括记录剂量,患者上一次使用的药物,当前检查中使用的药物,给药率和途径。
温特马克还说,需要对造影剂剂量进行跟踪,但在几年的时间里,在不同的位置进行成像时,很难跟踪。他说:“重要的是,我们收集这些信息,并把它们放在一起,希望最终我们能弄清事情的真相,了解到底发生了什么,我们希望能够在未来防止这种情况发生。”“我们需要收集这些信息,但这些信息要有帮助,就需要以严格的方式收集,因为我们不知道报告的症状是来自一个实体还是多个实体。这就是数据收集的质量对帮助理清问题非常重要的地方。”
放射学信息系统(RIS)和图像存档和通信系统(PACS)通常与造影剂没有接口,无法自动将信息传输到患者记录中,因此造影剂数据需要手动传输到系统中,Joanne Hoener说,她现在是拜耳公司的临床营销专家,并在RSNA的一次关于加放疗安全性的午间会议上发表了讲话。“当你手动操作时,你会得到不协调,”她说。对于MRI对比,Hoener说需要记录的是剂量率、强度、时间/日期、注射的药物和注射对比的设备。她说,出于各种原因,包括未来的数据挖掘,这些信息无论如何都应该记录在患者的记录中。
霍纳说:“我们谁也没有预料到钆沉积会成为一个问题,在2010年,它甚至没有出现在我们的雷达上。”“我们需要记录我们使用的造影剂和剂量,因为今天是钆,但明天可能是另一种类型的制剂。现有技术可以精确地改进对比文档,并通过删除手动文档步骤来改进工作流程。你使用什么供应商并不重要,重要的是文档。”
拜耳医疗保健的辐射和对比剂量跟踪Radimetrics平台是第一个也是最全面的跟踪系统之一。Sectra最近发布了一个用于CT和MRI试剂的对比跟踪系统。Guerbet在RSNA 2017上还发布了一款新的CT对比跟踪软件解决方案,并表示将在2018年扩展到MRI钆跟踪。
放射科是否需要钆检查知情同意书?
声称自己受到钆剂伤害的患者经常辩称,他们从未得到任何形式的知情同意文件,要求他们签署警告他们钆的潜在危险的文件。在RSNA 2017大会上发言的专家表示,这可能说起来容易做起来难。主要原因是大多数关于这些药物的临床数据表明它们是安全的。
“我不认为这是必要的,也没有理由,”卡纳尔说。“两名医疗事故律师告诉我,如果我只是告诉病人没有已知风险,但谁知道未来会发生什么,我们就无法获得知情同意——这不是知情同意。新的试验将有助于决定未来是否需要知情同意。”
阿加瓦尔说,一些诊所正在研究知情同意文件,但另一些诊所不希望这样做,因为担心这可能会引发诉讼。
取代钆剂
一些MRI供应商已经在吹捧黑血成像等新技术,或者可以减少或消除MRI对比需求的新协议。然而,温特马克说,一些类型的检查仍然需要使用钆来回答MRI应该回答的临床问题。
“目前有很多事情只能用钆造影剂来做。当利用对比剂填满血管来突出它们的事实时,还有其他技术可以使用。但是当观察肿瘤的腮红对比时,这是你用其他技术无法做到的具有相同的敏感性和特异性。目前正在进行寻找替代品的研究,但目前还没有好的替代品来替代钆可以帮助解决的所有问题。”
MRI钆安全问题相关内容
视频:MRI钆在大脑和身体中的滞留有多严重?麦克斯·温特马克医学博士访谈
视频“RSNA 2017年MRI钆造影剂安全性仍然备受关注,”采访伊曼纽尔·卡纳尔医学博士
线性GBCAs:
•Ablavar (gadofosset trisodium)
Eovist (gadoxetate二钠)
•磁石(gadopentetate dimeglumine)
•MultiHance (gadobenate dimeg)
•Omniscan(钆二胺)
•OptiMark (gadoversetamide)
大环的GBCAs:
•多特瑞姆(加朵酸葡胺)
•Gadavist (gadobutrol)
•ProHance (gadoteridol)
引用:
3.美国食品药品监督管理局药物评价与研究中心医学影像药物咨询委员会会议纪要。2017年9月8日会议。
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/Drugs/MedicalImagingDrugsAdvisoryCommittee/UCM579464.pdf。2018年2月16日访问。会议纪要:
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/Drugs/MedicalImagingDrugsAdvisoryCommittee/UCM584442.pdf

 2022年9月6日
2022年9月6日