2012年1月13日消息——去年7月制造商Bracco Diagnostics自愿召回CardioGen-82后,美国食品和药物管理局(FDA)正在向医疗保健专业人员和公众更新正在进行的调查的初步结果。CardioGen-82由一个发生器组成,用于临床生产铷(Rb)-82氯化物注射液。CardioGen-82正电子发射断层扫描(PET)扫描是一种使用放射性药物评估心肌灌注的核医学扫描。
来自调查的初步信息表明,在某些临床地点使用CardioGen-82的不当是导致一些患者暴露于比通常与CardioGen-82扫描相关的更多辐射的原因。辐射暴露的增加是由于使用了含有过量浓度的锶-82 (Sr-82)和锶-85 (Sr-85)的CardioGen-82发生器洗脱液。发电机洗脱液中Sr-82和Sr-85的过量释放被称为“锶突破”。FDA认为,这种过度暴露不太可能对患者造成重大风险,尽管暴露于任何过度辐射都是不可取的。
2011年7月26日药品安全通信FDA表示,它发现CardioGen-82的生产程序存在缺陷。迄今为止,这些缺陷似乎与在一些患者中检测到的过度辐射暴露无关。被召回的CardioGen-82发电机在发货后正常运行,制造商对其进行了测试,以确定锶突破的潜在结构或功能原因。所有测试的发电机都没有显示出突破的迹象。FDA表示,它将继续与制造商合作,以解决他们的生产缺陷。
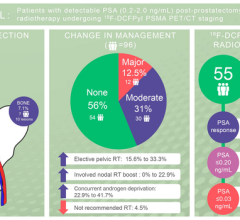
布拉科目前正在全国各地的临床地点进行研究,以帮助评估患者可能暴露于过度辐射的程度。本研究的参与是自愿的,初步数据显示,在43个临床站点调查的375名患者中,有54名患者因筛查试验结果异常而计划进行进一步的放射检测。所有54例患者来自两个临床站点。这两个地点似乎都没有充分的文件证明符合CardioGen-82锶突破检测标签建议。
FDA继续与制造商和其他联邦机构合作,以更好地描述导致某些临床场所患者过度辐射暴露的问题。FDA也正在与制造商合作,修订CardioGen-82标签,以更好地描述如何使用发生器,并实施计划CardioGen-82返回市场。FDA将在获得更多信息时向公众更新。

 2022年9月14日
2022年9月14日