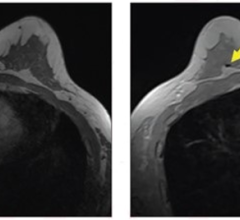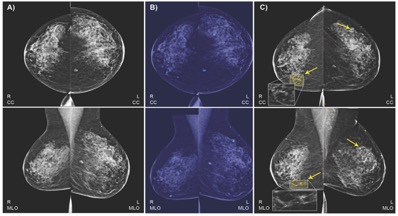
IBM收集了13234名女性的52936张图像数据集,这些女性在2013年至2017年期间至少做了一次乳房x光检查,在做乳房x光检查前至少有一年的健康记录。该算法对9611张乳房x光片进行了训练。图片由放射学提供。
2019年7月19日—乳腺癌是美国癌症相关死亡的全球主要原因女性,而最常被诊断出癌症在世界各地的妇女中从我们的角度来看,改善治疗方案和更早检测可能对降低死亡率产生积极影响,因为这可以在疾病仍处于早期阶段时为成功的干预和治疗提供更多的选择。
我们的IBM研究团队研究发表在放射学在一个新的人工智能(AI)该模型可以预测患者在一年内恶性乳腺癌的发展,其速度与人类放射科医生相当。作为同类算法中第一个从两者中学习并做出决策的算法图像数据综合病人的健康史,我们的模型能够正确预测其所分析病例中87%的乳腺癌的发展,也能够正确解释77%的非癌症病例。
我们的模型有一天可以帮助放射科医生确认或否认阳性乳腺癌病例。假阳性会导致大量的过度压力和焦虑,假阴性通常会阻碍癌症的早期发现和随后的治疗。
当对71个不同的病例进行测试时,放射科医生最初确定为“非恶性”,但最终在一年内被诊断为乳腺癌,我们的人工智能系统能够正确识别48%的个体(71个病例中的48%)的乳腺癌——否则这些患者不会被标记出来。
乳腺癌筛查的现状
目前,数字乳房x光检查是影像学筛查的主要方法。女性通常每1-2年接受一次乳房x光检查,这取决于她们的家族史。然后由放射科医生解释检查图像是否存在恶性发现。
分析乳房x光片是一项具有挑战性的任务。病灶和背景之间的差异可能非常细微:可能的发现有多种类型,它们在形状、大小、颜色、纹理和其他因素上彼此不同。由额外的放射科医生进行乳房x光片的二读检查已被证明能提高敏感性和特异性(2)。然而,在许多国家,由于缺乏训练有素的放射科医生和时间限制,往往很难将二读检查纳入标准筛查程序(3)。
为了帮助缩小现成的“第二读者”的差距,并帮助放射科医生进行分析,越来越多的系统正在转向基于深度神经网络的计算模型来分析医疗保健数据。
利用人工智能改善乳腺癌预测
我们的团队在IBM研究院-海法假设一个结合了机器学习和深度学习的模型可以被用于评估乳腺癌,其水平可以与放射科医生相媲美,并具有作为临床实践第二读者接受的能力。
与以色列最大的医疗保健机构之一合作,我们能够使用临床收集的、去识别的乳房x线摄影图像,这些图像还与每个患者的整体临床数据和生物标志物相关,如甲状腺功能、生殖史和其他信息。
利用这些信息,我们的团队能够创建一个独特而新颖的算法,据我们所知,这可能是第一个将乳房x光片和综合电子健康记录(EHR)数据结合起来预测乳腺癌的算法。基于深度学习模型,我们的团队能够训练该系统达到与放射科医生相当的准确性,这是美国筛查数字乳房x线照相术的基准标准所定义的。
此外,该模型描绘了其他临床风险特征之间的联系,如缺铁、白细胞分布、代谢综合征和甲状腺功能,并能够帮助降低研究病例中乳腺癌误诊的可能性。我们计划继续分析这些临床风险因素,以更好地了解它们的影响和与个人个性化风险的联系。
我们的机器学习算法之所以成功,很大程度上要归功于训练它们的大量数据。通过IBM的研究合作伙伴马卡比健康服务公司和阿苏塔医疗中心,这两家以色列的大型医疗服务提供商,我们的团队能够获得大量去识别的、自愿收集的乳房x光造影图像,这些图像还与相应个体的丰富而详细的临床数据记录相关联,如任何癌症诊断史、怀孕史和更年期状态。
此外,这些数据还包括活组织检查的随访、癌症登记数据、实验室结果和各种其他程序和诊断的代码。这些惊人的数据量为我们的机器学习模型提供了一个深度的信息库,并使这些算法能够将模式和趋势联系起来,这在其他情况下可能是不可能的。
为什么事情没有那么简单
在训练模型时,我们面临的最大挑战之一是将来自三个不同来源的数据结合起来。除了格式不同之外,临床数据经常有噪声或缺失值。此外,我们还想在算法中模拟放射科医生的典型决策过程。
例如,我们想使用两种标准视图,双侧颅侧(CC)和中外侧斜(MLO)视图,其中可能包括常规筛查乳房x线摄影。在全球的标准实践中,放射科医生在评估病变时通常会比较这两种观点,我们希望我们的模型也能以这种方式工作。
在此回顾研究我们收集了一个数据集,共52936张图片,来自13,234名女性,她们在2013年至2017年期间至少接受过一次乳房x光检查,在接受乳房x光检查前至少有一年的健康记录。我们对9,611张乳房x线照片和女性健康记录进行了算法训练,目的有两个:预测活检恶性肿瘤,区分正常与异常筛查检查。
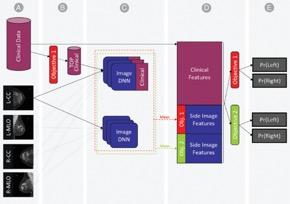
我们为这些目标创建了一个结合机器和深度学习的模型,使用乳房x光检查的标准四视图图像和详细的临床病史作为输入。
我们首先确定了对活检阳性预测贡献最大的临床特征子集。这些信息被融合到一个深度神经网络(DNN)中,该网络针对每个预测任务对每个乳房x光片进行训练。利用DNN,我们提取每个预测任务的概率,以及每个视图的成像特征。最后,我们将两种视图的成像特征以及一整套临床特征连接到患者乳房的单一表征中。肿瘤活检阳性或正常/异常分化的最终概率由梯度增强机模型估计。
好的结果和一些惊喜
我们的模型得到了接收器工作曲线(AUROC)下的面积为0.91,特异性为77.3%,灵敏度为%。在乳房x线照片中添加临床数据显著提高了模型的AUROC和灵敏度。
在仅基于临床数据的情况下,我们的模型AUROC为0.78,与Gail模型等常见风险模型相比,提高了乳腺癌风险预测能力。此外,我们能够确定可能导致风险升高的临床因素,以及以前其他模型没有使用的因素,如白细胞图谱和甲状腺功能测试。
更准确的预测有可能减少传统模式送去做不必要的检查的妇女人数,或因被不必要地列为高风险而遭受创伤的妇女人数。结合临床数据和影像学信息可以提供更准确验证初始结果的潜力。
来源
1.《全球癌症事实与数据》第三版。亚特兰大:美国癌症协会;2015.
2.https://pubs.rsna.org/doi/full/10.1148/radiol.2018171010
3.Leivo T, Salminen T, Sintonen H等。增加双读乳房x光片的成本效益。乳腺癌治疗1999;54(3):261-267
参考
放射学,将深度学习应用到关联的健康记录和乳房x光摄影图像中预测乳腺癌、Ayelet Akselrod-Ballin*、Michal Chorev*、Yoel Shoshan、Adam Spiro、Alon Hazan、Roie Melamed、Ella Barkan、Esma Herzel、Shaked Naor、Ehud Karavani、Gideon Koren、Yaara Goldschmidt、Varda Shalev、Michal Rosen-Zvi、Michal Guindy
Michal Chorev是IBM研究院的研究人员。


 2022年9月21日
2022年9月21日